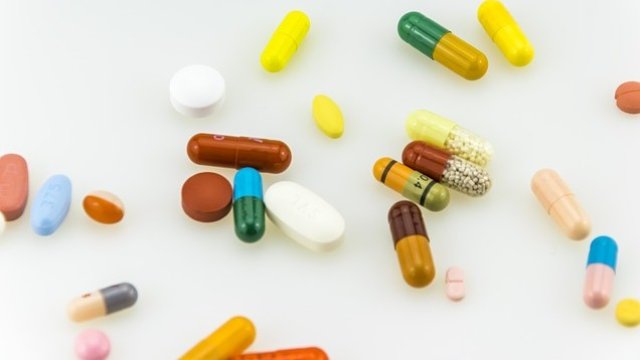
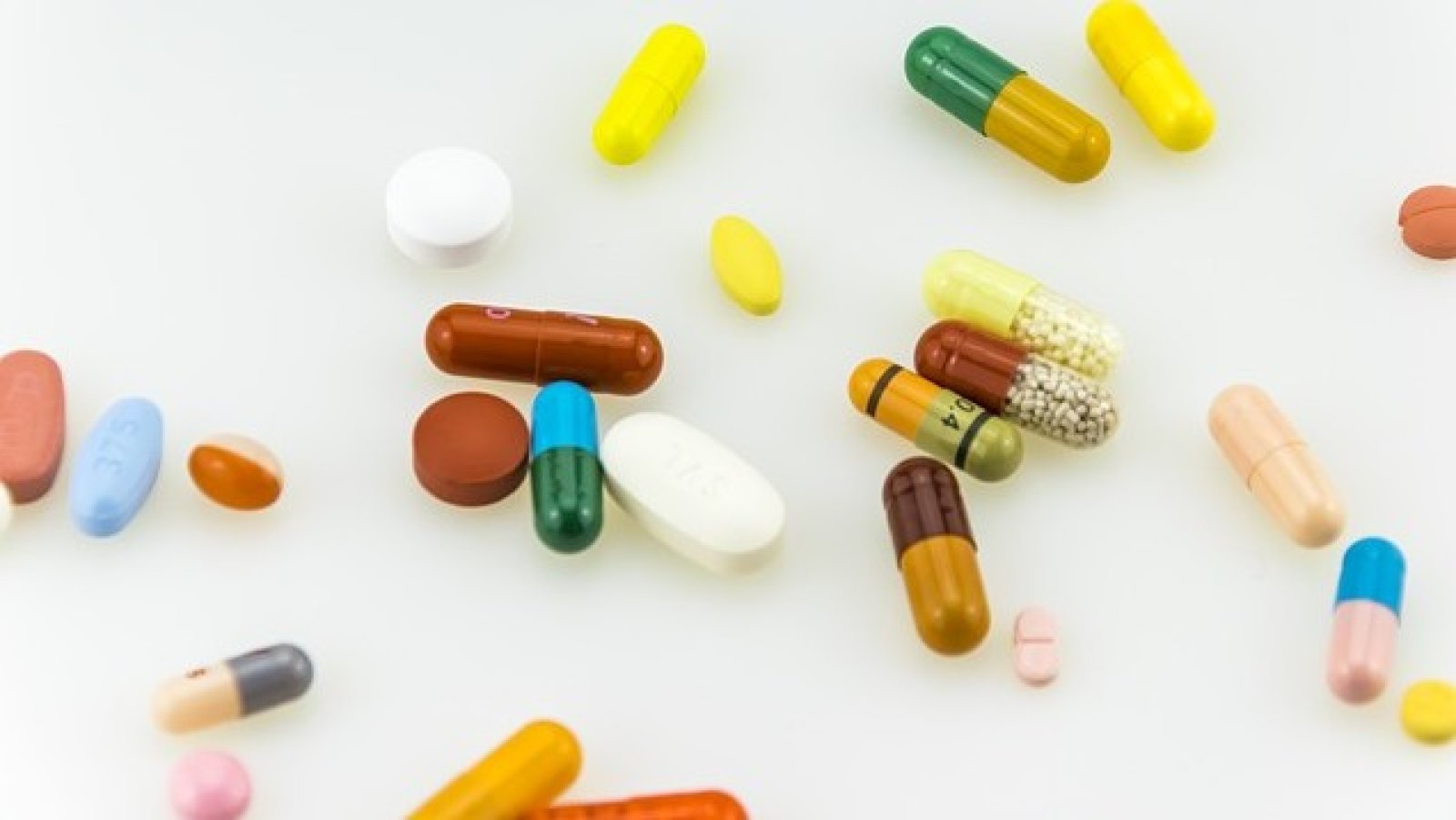
Създава се регламент, който прецизира употребата на лекарствата off-label (разрешено за употреба лекарство, което не отговаря на условията, дефинирани в разрешението за употреба, бел.ред.). Това става ясно от проекта за изменение и допълнение на наредба за условията и реда за лечение с неразрешени за употреба в Република България лекарствени продукти и лекарствени продукти за състрадателна употреба. Проектът е публикуван за обществено обсъждане.
Проектът урежда процедурата при употреба на лекарствени продукти извън условията на разрешението за употреба на подзаконово нормативно ниво.
Предвижда се предписването на лекарствения продукт, прилаган извън условията на разрешението за употреба, да се извършва с протокол, като към него да се прилага и писмено информирано съгласие на пациента, получено по реда на Закона за здравето.
Целта на измененията в наредбата е да се уреди процедурата при тяхната употреба.
„Off-label предписването е част от медицинската практика и може да е необходимо, за да се отговори на нуждите на отделните пациенти, поради липсата на подходящи разрешени алтернативи. Този вид употреба на лекарствени продукти понякога е единствената възможност за лечение на пациента и в този смисъл целта на наредбата е да гарантира проследяването на безопасността и ефикасността на лечението, както и информираността на пациента за прилаганата му терапия“, пише в мотивите към проекта.
В проекта е заложено и на пациента да му бъде предоставяна писмена информация, съдържаща причините за предписване на лечение с лекарствения продукт, прилаган извън условията на разрешението за употреба, наличието на научни доказателства, на които се базира употребата на лекарствения продукт при съответното показание, въпросите, по които липсва информация във връзка с употребата на лекарствения продукт, очакваните резултати и възможните рискове при лечението, начинът на прилагане, продължителността на лечението и условията за прекратяване на лечението.
С цел обезпечаване безопасността на пациентите се създава задължение медицинските специалисти, провеждащи лечението, да съобщават на притежателя на разрешението за употреба или на ИАЛ всички получени нежелани лекарствени реакции при употребата на лекарствен продукт, прилаган извън условията на разрешението за употреба.
„Като резултат от приемането на проекта се очаква правната рамка, която поставя българското законодателство в областта на лекарствените продукти, да обхване всеки аспект в тази област, за да не останат непосрещнати медицински нужди на българските пациенти. На следващо място с детайлизиране на уредбата, касаеща провеждане на лечение с лекарствен продукт, прилаган извън условията на разрешението за употреба се създават допълнителни гаранции, за да се опазят живота и здравето на пациентите и да се защитят техните права“, пише в мотивите към проекта.







 Мъж стреля след скандал с младежи в София
Мъж стреля след скандал с младежи в София  Първи заразен с хантавирус в Румъния
Първи заразен с хантавирус в Румъния  Си Дзинпин ще посети САЩ през есента
Си Дзинпин ще посети САЩ през есента  Мотористи протестираха с шествие по два лъча във Варна
Мотористи протестираха с шествие по два лъча във Варна  Конкурс на Обсерваторията във Варна е част от честванията по случай Международния ден на светлината
Конкурс на Обсерваторията във Варна е част от честванията по случай Международния ден на светлината 
 продава, Едностаен апартамент, 58 m2 Бургас, Възраждане, 119000 EUR
продава, Едностаен апартамент, 58 m2 Бургас, Възраждане, 119000 EUR  продава, Тристаен апартамент, 116 m2 София, Младост 4, 289925 EUR
продава, Тристаен апартамент, 116 m2 София, Младост 4, 289925 EUR  продава, Двустаен апартамент, 64 m2 Бургас област, к.к.Слънчев Бряг, 84900 EUR
продава, Двустаен апартамент, 64 m2 Бургас област, к.к.Слънчев Бряг, 84900 EUR  продава, Двустаен апартамент, 47 m2 Бургас област, к.к.Слънчев Бряг, 56500 EUR
продава, Двустаен апартамент, 47 m2 Бургас област, к.к.Слънчев Бряг, 56500 EUR  продава, Къща, 207 m2 Пловдив област, с.Белащица, 189000 EUR
продава, Къща, 207 m2 Пловдив област, с.Белащица, 189000 EUR 
 Никола Янков: Новото правителство може да пропилее репутационния бонус от еврото
Никола Янков: Новото правителство може да пропилее репутационния бонус от еврото  ОАЕ ще удвоят капацитета си за износ на петрол извън Ормузкия проток до 2027 г.
ОАЕ ще удвоят капацитета си за износ на петрол извън Ормузкия проток до 2027 г.  Honda и Nissan може да подновят разговорите за обединение
Honda и Nissan може да подновят разговорите за обединение  Печелившите и губещите от срещата на върха на Тръмп и Си Дзинпин в Пекин
Печелившите и губещите от срещата на върха на Тръмп и Си Дзинпин в Пекин  Китайската икономика започва поредно тримесечие с дивергенция на растежа
Китайската икономика започва поредно тримесечие с дивергенция на растежа 
 Ето как новият модел на BYD върви на три колела
Ето как новият модел на BYD върви на три колела  Музеен експонат отнесе глоба за превишена скорост
Музеен експонат отнесе глоба за превишена скорост  Цялата гама на MINI с 5 звезди от Euro NCAP
Цялата гама на MINI с 5 звезди от Euro NCAP  Провали ли се наистина електромобилът?
Провали ли се наистина електромобилът?  Zeekr стъпва на българския пазар с първи официален дилър
Zeekr стъпва на българския пазар с първи официален дилър 
 Светът изгаря своята мрежа за сигурност от петрол
Светът изгаря своята мрежа за сигурност от петрол  Джей Ло видимо флиртува с колегата си Брет Голдщайн
Джей Ло видимо флиртува с колегата си Брет Голдщайн  Престъпници на фронта: Броят на затворниците в Русия намалял с 40%
Престъпници на фронта: Броят на затворниците в Русия намалял с 40%  Дори Сатаната не може да спаси Владимир Путин
Дори Сатаната не може да спаси Владимир Путин  Пеканов: Проблемите покрай еврото у нас са от безвремието и безвластието
Пеканов: Проблемите покрай еврото у нас са от безвремието и безвластието 
























